中国科学院脑科学与智能技术卓越创新中心网站消息,2023年11月9日24点,《Cell》期刊以封面文章的形式在线发表题为《Live birth of chimeric monkey with high contribution from embryonic stem cells》(高比例胚胎干细胞贡献的出生存活嵌合体猴)的研究论文。该研究由中国科学院脑科学与智能技术卓越创新中心(神经科学研究所)、上海脑科学与类脑研究中心刘真研究组、脑智卓越中心非人灵长类研究平台孙强研究团队和中国科学院广州生物医药与健康研究院Miguel A. Esteban研究组合作完成。该研究在国际上首次成功构建了高比例胚胎干细胞贡献的出生存活嵌合体猴,并证实了猴胚胎干细胞可以高效的贡献到胚外胎盘组织和生殖细胞。这对于理解灵长类胚胎干细胞全能性具有重要意义,为遗传修饰模型猴的构建奠定了技术基础。
胚胎干细胞是指由着床前囊胚的内细胞团在体外分离培养而来的多能性细胞,在模式动物构建、细胞治疗、器官再生、类器官模型等生物医药领域发挥着重要作用。胚胎干细胞具有体外无限自我复制更新、诱导实现多向分化、胚胎注射形成嵌合体等关键特征,其中胚胎注射形成嵌合体被公认为是评估胚胎干细胞多向分化潜能的金标准。
小鼠胚胎干细胞注射到囊胚并形成嵌合体的技术是构建遗传修饰小鼠模型的关键技术。1984年首次实现小鼠胚胎干细胞胚胎注射形成嵌合体,2008年成功实现大鼠胚胎干细胞胚胎注射形成嵌合体。建立非人灵长类胚胎干细胞嵌合体技术对于生物医药研究具有非常重要的意义,然而非人灵长类胚胎干细胞嵌合体研究一直进展缓慢。
该研究的首要问题在于获得具有高效发育潜能的胚胎干细胞。针对这一问题,研究团队建立了处于6种不同培养体系下的食蟹猴胚胎干细胞,进而从克隆形态、免疫荧光、单细胞转录组、线粒体代谢、全基因组甲基化、核型分析和全基因组测序等多方面对处于不同培养条件下食蟹猴胚胎干细胞进行全面系统的评估。发现5iLAF、4CL和PXGL体系下培养的食蟹猴胚胎干细胞具有较高的多能性,而且4CL体系下的干细胞具有更好的传代稳定性和基因组稳定性。
胚胎干细胞注射入受体胚胎后的快速凋亡是影响胚胎干细胞成功嵌合的关键。研究团队选用绿色荧光蛋白标记的4CL条件下的胚胎干细胞进行猴胚胎注射实验,通过测试干细胞注射入胚胎后的不同培养基和培养时间的组合,最终得到了既不影响胚胎正常发育又能保证干细胞存活的最优嵌合胚胎培养条件。而且5iLAF和Primed体系下的胚胎干细胞在该优化条件下也表现出胚胎注射后的高存活率。将注射了4CL和5iLAF干细胞的嵌合胚胎分别在体外延迟培养到第17天,发现注射的胚胎干细胞仍然可以高效存活,单细胞测序表明猴胚胎干细胞可以与受体胚胎细胞同步发育,并且贡献到第17天猴胚胎的不同细胞谱系中。
在系统性评估了不同培养条件下猴胚胎干细胞状态和改进优化了嵌合胚胎培养条件的基础上,研究团队进一步将注射了绿色荧光标记的4CL干细胞的胚胎移植到代孕母猴。在总共得到的10只出生或流产的仔猴中,有一只出生存活猴和一只流产猴检测到胚胎干细胞的嵌合。研究团队建立了包含PCR扩增、微卫星亲子鉴定、基因组单核苷酸多态性深度测序、流式细胞仪检测、绿色荧光蛋白检测、免疫荧光检测的一系列严格的嵌合体分析流程,发现出生存活猴中胚胎干细胞的贡献比例高达70%左右,流产猴中胚胎干细胞的贡献比例约20%。单细胞转录组测序也进一步表明了注射的胚胎干细胞可以跟受体胚胎细胞同步分化到出生个体猴的各种不同细胞谱系中。
胎盘组织和生殖细胞是胚胎发育和重编程过程中的两类特殊组织或细胞。其中胎盘组织是由滋养外胚层发育而来,而生殖细胞发育过程中要经历更加剧烈的表观重编程。研究团队在两只嵌合体猴的胎盘组织中均发现了胚胎干细胞的高比例贡献。考虑到小鼠胚胎干细胞几乎不会贡献到胎盘组织,该结果说明灵长类胚胎干细胞可能具有不同于啮齿类的独特的发育全能性特征。此外两只嵌合体猴的生殖细胞中也发现了胚胎干细胞的高比例贡献,这对后续基于该技术的遗传修饰模型构建至关重要。
该工作建立了系统评估不同培养条件下猴胚胎干细胞的多能性状态的研究体系,并探索得到有利于胚胎干细胞存活的胚胎嵌合体的培养条件,显著提升了胚胎干细胞注入胚胎后的存活效率,最终得到了出生存活的高比例胚胎干细胞贡献的嵌合体猴,证实了注入的猴胚胎干细胞可以高效地贡献到包括胎盘和生殖细胞在内的各种不同组织和细胞。该研究对于理解灵长类胚胎干细胞全能性和发育潜能具有重要意义,为建立基于猴胚胎干细胞嵌合体的基因打靶和模型构建技术奠定了基础。
该研究严格遵守生物伦理规范,所有实验均符合国际干细胞研究学会的研究指南,并经过脑智卓越中心伦理委员会审核。中国科学院脑智卓越中心刘真研究员、孙强研究员和中国科学院广州生物医药与健康研究院Miguel A. Esteban研究员为该论文共同通讯作者。中国科学院脑智卓越中心、西北农林科技大学联合培养博士研究生曹静、脑智卓越中心副研究员李杰、助理实验师李春杨、中国科学院广州生物医药与健康研究院副研究员李文娟、Md. Abdul Mazid、博士研究生贾雯淇、吉林大学博士研究生姜禹为该论文共同第一作者。该研究还得到了脑智卓越中心蒲慕明院士、西北农林科技大学王小龙教授、华大生命科学研究院徐讯研究员和刘龙奇研究员、剑桥大学Patrick Maxwell教授、以及脑智卓越中心、广州健康院、华大生命科学研究院多位合作同事的大力支持。该研究得到了脑智卓越中心光学成像平台和分子细胞技术平台的技术支撑。该研究获得了科技部、中国科学院、上海市、基金委的资助。
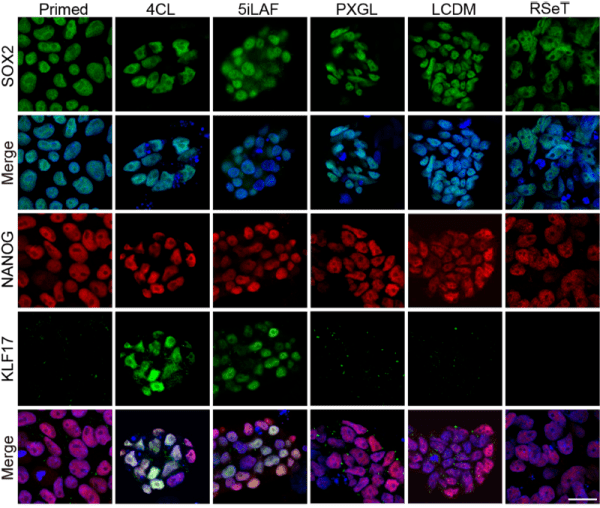
图1.不同培养条件下猴胚胎干细胞中SOX2,NANOG和KLF17的免疫荧光。
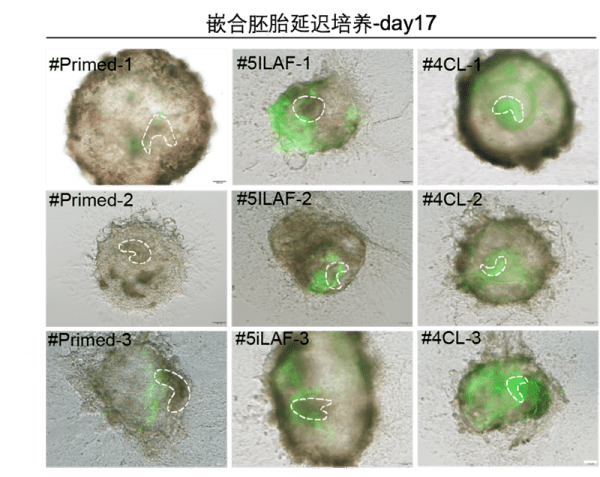
图2.不同细胞注射的嵌合胚胎体外延迟培养效果图。
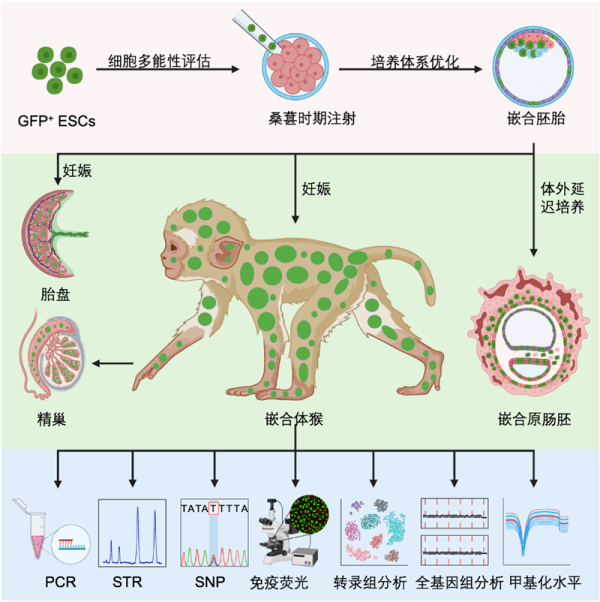
图3. 非人灵长类胚胎干细胞嵌合体研究模式图。
图4. 胚胎干细胞嵌合体猴卡通寓意图被选为该期Cell杂志的封面。

图5. 胚胎干细胞嵌合体猴研究团队主要成员(左起:李杰、曹静、刘真、孙强、李春杨)